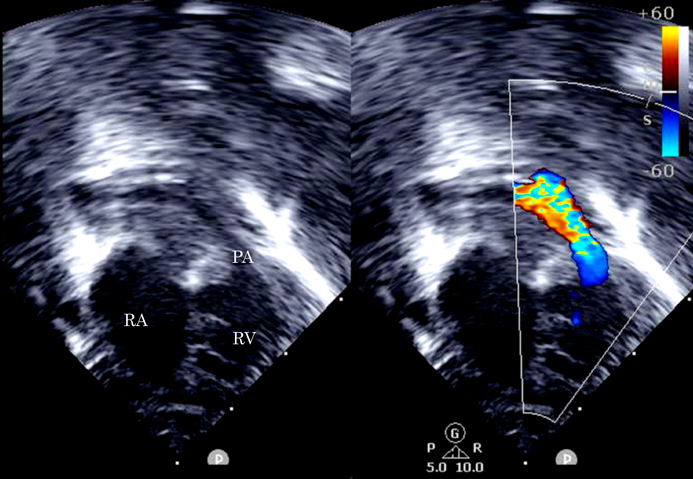
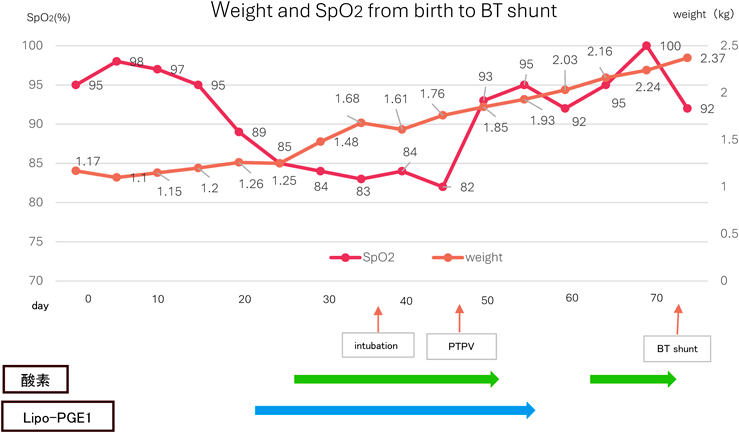
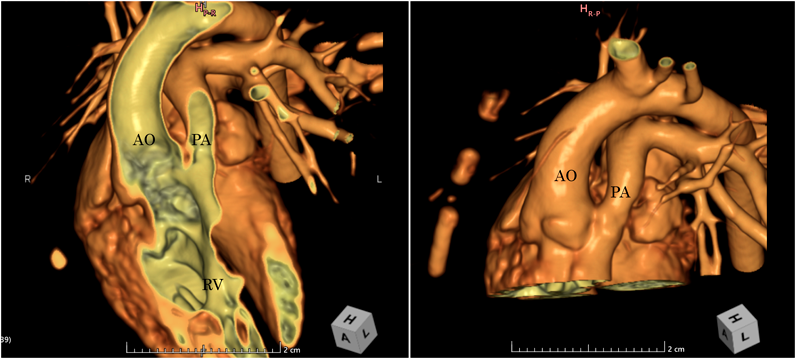
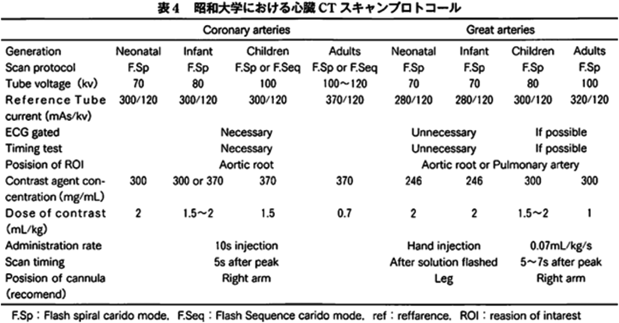
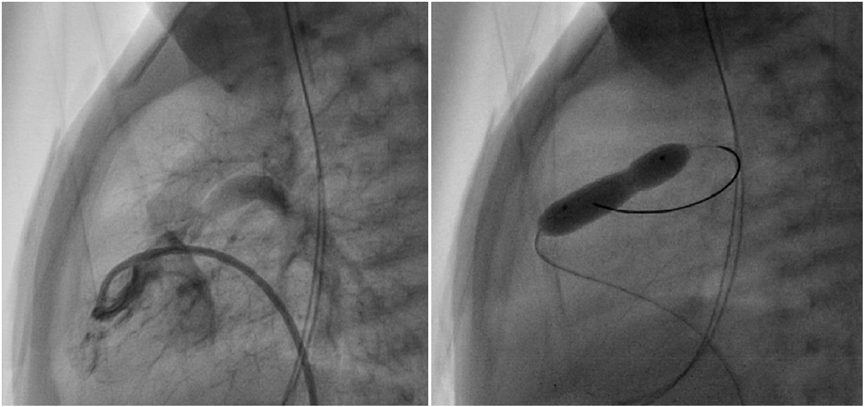
動画化した全時相造影CTが経皮的肺動脈弁形成術(PTPV)効果予測に有用だった:両大血管右室起始症の一例Full-time contrast enhanced CT with moving images predicts efficacy of percutaneous pulmonary transluminal valvuloplasty for double-outlet right ventricle: A case report
石井 瑶子,大山 伸雄,加藤 真理子,山岡 大志郎,堀川 優衣,長岡 孝太,清水 武,堀尾 直裕,喜瀬 広亮,藤井 隆成,富田 英Yoko Ishii, Nobuo Oyama, Mariko Kato, Daishiro Yamaoka, Yui Horikawa, Kota Nagaoka, Takeshi Shimizu, Naohiro Horio, Hiroaki Kise, Takanari Fujii, Hideshi Tomita
昭和大学病院 小児循環器・成人先天性心疾患センターSHOWA University Hospital
受付日:2023年9月27日Received: September 27, 2023
受理日:2023年12月18日Accepted: December 18, 2023
発行日:2024年1月24日Published: January 24, 2024