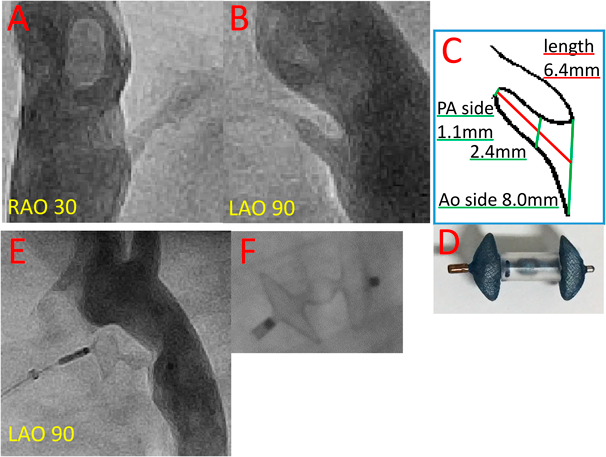
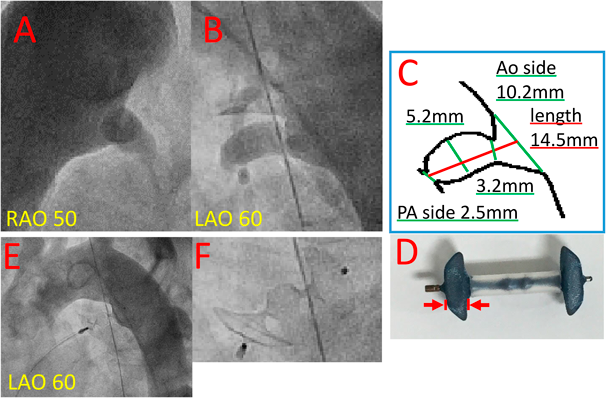
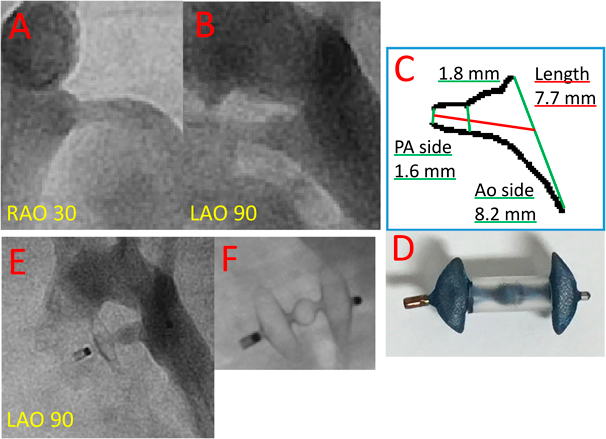
Amplatzer™ Duct Occluder (ADO) IIのデバイス特性に関する検討 —どのような動脈管に対してADO IIを用いるべきか—The Characteristics of the Amplatzer™ Duct Occluder (ADO) II—What type of patent ductus arteriosus is feasible for ADO II ?—
1 山梨大学医学部小児科Department of Pediatrics, Faculty of Medicine, University of Yamanashi
2 昭和大学小児循環器・成人先天性心疾患センターPediatric Heart Disease & Adult Congenital Heart Disease Center, Showa University Hospital